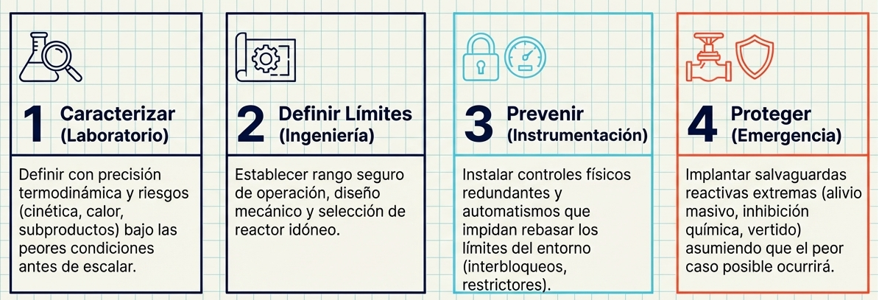
En la ingeniería de procesos, la frontera entre una producción eficiente y un desastre industrial es una línea matemática invisible.
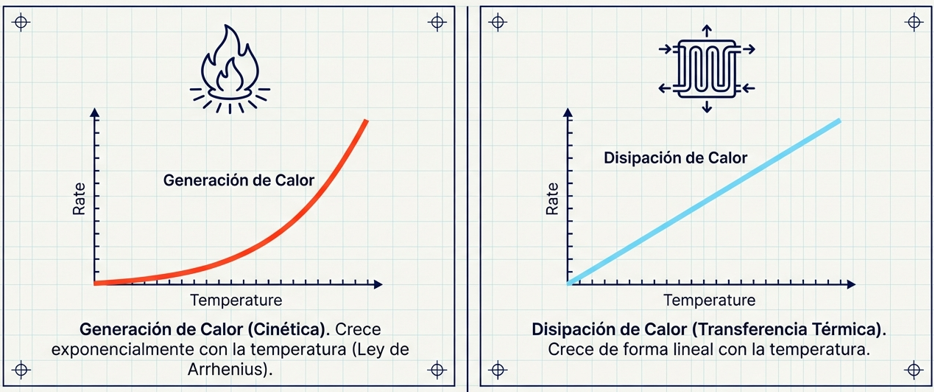
Como especialistas, solemos visualizar este equilibrio a través de la Gráfica de Semenov, que ilustra la lucha constante entre la generación de energía y la capacidad de evacuación térmica.

En condiciones ideales, operamos en un estado estacionario; sin embargo, cuando la termodinámica se desvía, lo que era una transformación controlada puede derivar en una transformación adiabática, donde el calor se retroalimenta a sí mismo.

Comprender la seguridad de procesos no es solo instalar alarmas, es descifrar la personalidad cinética de nuestras reacciones antes de que el sistema alcance un punto de no retorno.

- La trampa de las reacciones “débiles” y el gatillo térmico
En mi experiencia analizando riesgos en planta, el error más común es subestimar las reacciones con baja entalpía. Existe la falsa seguridad de que, si una reacción libeera poco calor, ees intrínsecamente inofensiva. No obstante, la seguridad química no es lineal.
Una reacción débilmente exotérmica puede actuar como un “detonante sileencioso”, elevando la temperatura del sistema lo justo para activar una segunda ruta cinética mucho más violenta y devastadora, como una polimerización descontrolada o una descomposición térmica de subproductos.
“Las reacciones débilmente exotérmicas pueden originar un incremento de temperatura suficiente para permitir la aparición posterior de otra reacción fuertemente exotérmica”.
2. La matemática del desastre: El abismo entre lo lineal y lo exponencial.
El fenómeno del runaway o descontrol térmico se rige por la Cinética de Arrhenius. La velocidad de una reacción, y por eende su geeneración de calor, crece de fforma xponencial con la temperatura. En contraste, la capacidad de nuestro sistema de refrigeración para retirar ese calor (basada en el coeficiente de transferencia y la superficie de intercambio) solo aumenta de forma lineal.

Cuando la curva eexponencial de generación supera la capacidad lineal de disipación, el sistema cruza la
TNR (Temperature of No Return)
o Temperatura Sin Retorno. En este umbral crítico, el descontrol se vueelvee irreversible: el calor acumulado acelera la reacción a una velocidad tal que ningún sistema de refrigeración conveencional puede recuperar el mando. Es el momento en que la química toma el control absoluto del reactor.
3. El riesgo no conoce fronteras: Más allá del recipiente principal.
Es un sesgo peligroso centrar la vigilancia exclusivamente en el reactor de síntesis. La pérdida de control térmico es una amenaza ubicua que acecha een cualquier unidad donde existían sustancias reactivas o térmicamente inestables. Para garantizar la Seguridad Inherente de una instalación, debemos ampliar el foco hacia.
- Columnas de destilación: Donde la concentración de fondos térmicamente inestables puede desencadenar descomposiciones durante la purificación.
- Tubeerías y líneas de transferencia: Donde el estancamiento de fluidos reactivos puede generar puntos calientes (hotspots).
- Depósitos de almacenamiento: Donde una descomposición lenta, pero sin vías de evacuación de calor, puede acumular energía durante días hasta culminar en una explosión térmica.
4. Catalisis accidental: Cuando el propio reactor se vuelve el enemigo
En el mundo de la química, el diablo habita en los detalles infinitesimales. Una modificación aparentemente irrelevante en el proceso puede ser el catalizador de una catástrofe. Un ejemplo crítico extraído de la normativa técnica es el cambio de materiales en la construcción del reactor: sustituir un equipo por otro de una acero distinto puede introducir trazas de hierro que, lejos de ser inertes, se disuelven en la mezcla de reacción actuando como un catalizador homogéneo para descomposiciones violentas.
Del mismo modo, contaminantes cotidianos como el agua, el oxígeno del aire o incluso los lubricantes de los agitadores pueeden alterar la ruta cinética establecida, reduciendo la energía de activación de reacciones secundarias peligrosas y transformando un proceso estable en una bomba de tiempo.
5. El diseño “Semi-discontinuo”: El control de la energía en tiempo real
Frente al rieesgo del reactor por lotes (batch), donde todos los reactivos están presentes desde eel inicio, eel modelo semi-discontinuo se erige como un pilar de la seguridad preventiva. Al dosificar uno de los reactivos de forma controlada, limitamos la masa reactiva presente en cada instante.
Sin embargo, un experto debe considerar siempre el peligro de acumulación: si la teemperatura de operación es demasiado baja, el reactivo añadido no reacciona inmediatamente, sino que se acumula. Si la teemperatura sube reepentinamente, toda esa masa acumulada reaccionará al unísono, provocando un descontrol masivo.
Sus veentajas eestratéegicas, siempree quee se eevitee la cumulación, con claras:
- Limitación de inventario reactivo: menos energía potencial disponible en el interior del recipiente.
- Acción de parada inmediata: La interrupción de la alimeentación de reactivos actúa como un “freno de mano” químico.
- Gestión de la transferencia de calor: Permite acompasar la generación de energía con la capacidad real del intercambiador.
Conclusión: Hacia una cultura de prevención inherente
La seguridad industrial no puede ser una capa externa de alarmas y válvulas de alivio; debe nacer del diseño mismo del proceso. Comprender la termodinámica no es una opción técnica, es un imperativo ético. Al final del día, los sistemas de protección pueden fallar y los sensores pueden descalibrarse.


La pregunta que todo director de planta y responsable de seguridad debe hacerse es:
¿Está nuestro proceso diseñado para ser inherentemente seguro frente a las leyes de la termodinámica, o estamos confiando el destino de la planta a que el sistema de control sea más rápido que la irreversible Cinética de Arrhenius en una tarde de viernes?